
长时间的清醒状态会导致持续且深度的恢复性睡眠(RS)。然而,调节这一过程的神经元回路仍不明确。
2025年6月19日,约翰斯·霍普金斯大学Mark N. Wu团队在Science 在线发表题为“Sleep need–dependent plasticity of a thalamic circuit promotes homeostatic recovery sleep”的研究论文,该研究通过在小鼠身上进行的回路筛选,发现了一组在睡眠剥夺(SD)期间被激活的丘脑联合核(RE)神经元,这些神经元对于睡眠稳态至关重要。
对 RE 神经元进行光遗传学激活会产生一种异常的表型:在睡眠前的行为(如梳理和构建巢穴),随后是长时间且强烈的睡眠,这种睡眠类似于 RS。在睡眠剥夺期间抑制 RE 活性会损害随后的 RS,这表明这些神经元传递睡眠需求信号。RE 神经元位于促进睡眠的区带不定细胞的上游,而睡眠剥夺会触发该回路的可塑性,以增强它们的连接性。这些发现揭示了一种回路机制,通过这种机制,睡眠需求会改变睡眠回路的功能耦合,从而促进持续、深度的睡眠。

睡眠受到内稳态机制的调控:在长时间的清醒之后,动物会进入持续、连贯且深度的睡眠状态。尽管过去一个世纪里对睡眠的内稳态调节机制进行了深入研究,但这一过程的生物学基础仍是个谜。目前正有进展在阐明调节睡眠的分子途径。相比之下,感知并/或传递内稳态睡眠信号的神经回路的特性尚不清楚。
在小鼠的神经回路上,研究人员发现了一个位于丘脑联合核(RE)内的兴奋性神经元群,它们向多个促进非快速眼动(NREM)睡眠的下游集群发送信号。对 RE 神经元进行短暂的光遗传学激活会导致一种罕见的表型——在延迟之后会出现持续、巩固且深度的 NREM 睡眠。值得注意的是,在入睡前的延迟阶段,这些动物会进行睡眠准备行为,包括梳理和筑巢。由于这种持续、巩固和深度的睡眠表型类似于睡眠剥夺后所观察到的稳态恢复睡眠,因此研究人员试图探究 RE 神经元是否参与睡眠的稳态调节。
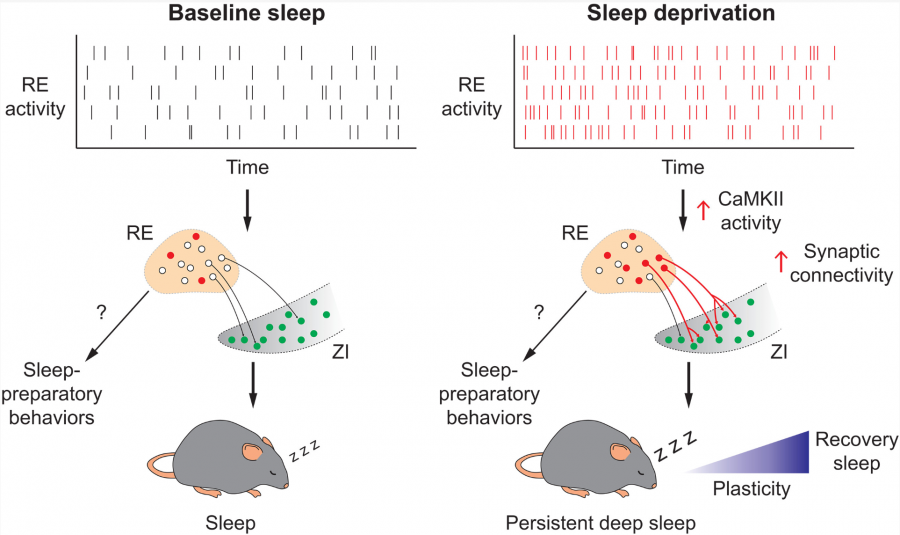
睡眠需求相关的 RE-ZI 神经回路的可塑性促进了稳态恢复性睡眠(图源自Science )
大多数促进 NREM 睡眠的神经元在 NREM 睡眠期间活动增强。为了测量 RE 神经元的体内活动,该研究在睡眠剥夺和恢复睡眠期间进行了长期的神经像素记录。这些记录显示,RE 活动在睡眠剥夺和/或清醒期间更强,在恢复睡眠期间则减弱。接下来,该研究检查了睡眠剥夺期间这种增强的 RE 活动是否是睡眠需求积累所必需的。在睡眠剥夺期间对 RE 神经元进行化学遗传学抑制会减少后续的稳态恢复睡眠量、睡眠巩固以及深度。
RE 神经元通过向位于锥状不定区(ZI)中先前已确定的促进 NREM 睡眠的簇发送信号来促进 NREM 睡眠。出乎意料的是,睡眠剥夺会导致 RE-ZI 连接的神经可塑性变化。这种 RE-ZI 可塑性的程度与后续的稳态恢复睡眠量相关。此外,这种突触可塑性增强了 RE 和 ZI 神经元簇之间的形态和功能连接。钙和钙调蛋白依赖性蛋白激酶 II(CaMKII)已被证实能够调节突触可塑性,并与睡眠的稳态调节有关。在 RE 神经元中抑制 CaMKII 活性会降低 RE-ZI 可塑性,并且由睡眠剥夺触发的后续稳态恢复睡眠也会受到抑制。
总之,该研究结果表明,RE 神经元对于睡眠需求的积累是必需的,并且能够产生持续的、深度的睡眠,类似于内稳态恢复睡眠。睡眠剥夺会促使 RE-ZI 神经回路发生可塑性变化,增强这一促进睡眠的模块的连接性。这种可塑性的程度与内稳态睡眠反弹的量相关,这表明 RE-ZI 可塑性充当了睡眠需求的分子读数。这些发现揭示了睡眠缺失如何通过改变睡眠回路的功能耦合来促进持续、深度睡眠的机制。
参考消息:
https://www.science.org/doi/10.1126/science.adm8203
原标题:熬夜后为啥睡得更香?《Science》揭秘睡眠开关的惊人可塑性
本文作者:枫叶,转载于微信公众号:iNature(ID:Plant_ihuman),转载引用请注明原出处